Tvorba močoviny. Neutralizace amoniaku. syntéza močoviny
Hlavním mechanismem pro neutralizaci amoniaku v těle je biosyntéza močoviny. Ten je vylučován močí jako hlavní konečný produkt metabolismu bílkovin, respektive aminokyselin. Močovina tvoří až 80–85 % veškerého dusíku v moči. Hlavním a možná jediným místem syntézy močoviny jsou játra. G. Krebs a K. Hanseleit poprvé odvodili v roce 1932 rovnice pro reakce syntézy močoviny, které jsou prezentovány ve formě cyklu, který dostal název v literatuře ornitinový Krebsův močovinový cyklus.
Nutno podotknout, že v biochemii se jednalo o první cyklický metabolický systém, jehož popis téměř o 5 let předcházel G. Krebsovi objev dalšího metabolického procesu, cyklu trikarboxylových kyselin. Další studie do značné míry potvrdily cyklickou povahu biosyntézy močoviny v játrech. Díky výzkumu G. Coena, S. Ratnera a kol. byly objasněny mezikroky a enzymové systémy, které katalyzují tvorbu močoviny.
Celý cyklus tvorby močoviny lze tedy znázornit následovně. V první fázi je syntetizována vysokoenergetická sloučenina karbamoylfosfát - metabolicky aktivní forma amoniaku používaná jako výchozí produkt pro syntézu pyrimidinových nukleotidů (respektive DNA a RNA) a argininu (respektive proteinu a močoviny):
Močovina je hlavním konečným produktem metabolismu dusíku, při kterém se z těla vylučuje přebytečný dusík.
Ornitinový cyklus v játrech plní dvě funkce:
Přeměna aminokyselin na močovinu, která se vylučuje a zabraňuje hromadění toxických produktů, zejména amoniaku;
Syntéza argininu a doplnění jeho fondu v těle.
Zvažte cyklus močoviny:
![]()
Obrázek 34- Ornitinový cyklus syntézy močoviny v játrech
Začíná to tvorbou karbamoylfosfátu v mitochondriích, kde je hodně ATP.
1 Tvorba karbamoylfosfátu. Amonné ionty vznikající oxidativní deaminací kyseliny glutamové interagují s hydrogenuhličitanovým aniontem a ATP za účasti karbamoylfosfátsyntetázy za vzniku karbamoylfosfátu obsahujícího makroergickou vazbu:
NH 4 + + HCO 3 - + 2ATP → H 2 N - C + 2ADP + H 2 RO 4 - + H +
Karbamoyl fosfát
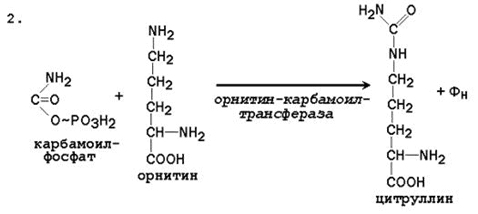
2. Získání citrulinu. V matrici mitochondrií kondenzuje karbamoylfosfát s aminokyselinou ornitinem, která jako homolog lysinu není obsažena v proteinech.
Reakce je katalyzována ornithinkarbamoyltransferázou:
H COO - O H COO -
C + H 2 N - C → CO + H 2 RO 4 -
+ / \ + \ + / \ ||
H3N (CH2)3NH30~ F H3N (CH2)3NH-C-NH2
Ornithin Carbamoyl Phosphate Citrulin
Vzniklý citrulin přechází do cytosolu jaterních buněk, kde probíhá zbytek reakcí močovinového cyklu.
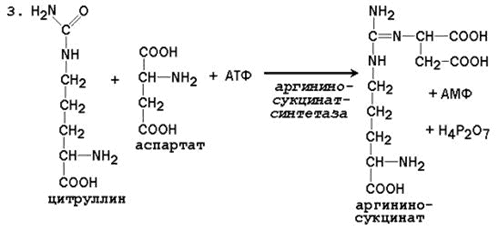
3. Získání argininosukcinátu. Nahrazení karbonylové skupiny citrulinu aminoskupinou aspartátu za vzniku guanidinové skupiny argininosukcinátu probíhá za účasti ATP a je katalyzováno argininosukcinátsyntetázou:
H COO - H COO -
C O + C + ATP →
H3N (CH 2) 3 NH - C - NH 2 H 3 N CH 2 COO -
citrulin aspartát
CH2NCH2COO- + H2P2072- + AMP
H3N (CH2)3NH - C - NH - SNSOO -
Argininosukcinát
Reakce je endergonická, na první a třetí reakci cyklu se spotřebují 4 molekuly ATP.
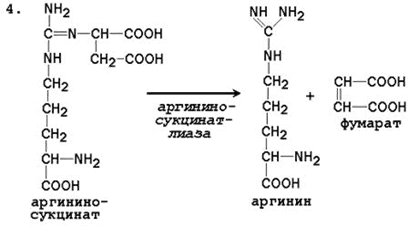
4. Rozpad argininosukcinátu. Působením argininosukcinátlyázy se argininosukcinát exergicky štěpí za vzniku argininu a fumarátu:
H COO - H COO - COO - N
CH2N CH2COO - → CH2N + C \u003d C
+ / \ || | + / \ || / \
H3N (CH 2) 3 NH - C - NH - SNSOO - H 3 N (CH 2) 3 NH - C - NH 2 H COO -
Argininosukcinát Arginin fumarát
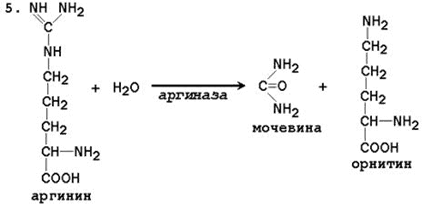
5. Tvorba močoviny a regenerace ornithinu. Hydrolýza argininu, katalyzovaná arginázou, vede k tvorbě močoviny a regeneraci ornithinu. Reakce je exergonická.
H COO - H COO - NH 2
CH2N → C + O \u003d C
+ / \ || + / \ + \
H3N (CH 2) 3 NH - C - NH 2 H 3 N (CH 2) 3 NH 3 NH 2
Arginin Ornitin močovina
Regenerovaný ornitin může opět vstoupit do mitochondrií a podílet se na novém obratu cyklu močoviny. Výsledná močovina je transportována z jater do ledvin, kde je extrahována z krve a vyloučena z těla močí.
V ornitinovém cyklu se na každý obrat cyklu spotřebují 4 makroergické vazby tří molekul ATP.
Proces tvorby močoviny si však dodává energii:
Při regeneraci aspartátu z fumarátu ve fázi dehydrogenace malátu vzniká NADH, který může zajistit syntézu 3 makroergických vazeb.
Při oxidativní deaminaci glutamátu v různých orgánech vzniká také NADH, který může zajistit syntézu 3 makroergických vazeb.
Z výše uvedených reakcí je vidět, že toxický amoniak se přeměňuje na neškodnou močovinu. V tomto případě je jeden z atomů dusíku močoviny tvořen z amoniaku, druhý z aspartátu.
24.4.1. Biosyntéza močoviny- hlavní způsob neutralizace čpavku. Močovina je syntetizována v ornitinovém cyklu v jaterních buňkách. Tento sled reakcí objevili H. Krebs a K. Henseleit v roce 1932. Podle moderních koncepcí zahrnuje močovinový cyklus sled pěti reakcí.
Dvě počáteční reakce biosyntézy močoviny probíhají v mitochondriích jaterních buněk.
Následné reakce probíhají v cytoplazmě jaterních buněk.
Obecné schéma ornitinového cyklu je znázorněno na obrázku 24.2:
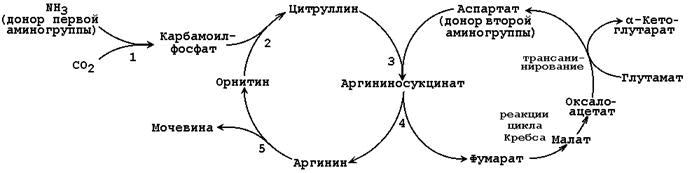
Obrázek 24.2. Schéma ornitinového cyklu a jeho vztah k přeměnám kyseliny fumarové a asparagové.
Čísla označují enzymy, které katalyzují reakce ornitinového cyklu: 1 - karbamoylfosfátsyntetáza; 2 - ornitin-karbamoyltransferáza; 3 - argininosukcinát syntetáza; 4 - argininosukcinát lyáza; 5 - argináza.
24.4.2. Ornitinový cyklus je blízko vztahy s cyklem trikarboxylových kyselin:
- počáteční reakce močovinového cyklu, stejně jako reakce TCA, probíhají v mitochondriální matrix;
- přísun CO2 a ATP, nezbytných pro tvorbu močoviny, je zajištěn prací CTC;
- v cyklu močoviny vzniká fumarát, který je jedním ze substrátů TCA. Fumarát je hydratován na malát, který je zase oxidován na oxaloacetát. Oxalacetát může podstoupit transaminaci na aspartát; tato aminokyselina se podílí na tvorbě argininosukcinátu.
24.4.3. Regulace aktivity enzymů cyklus probíhá především na úrovni karbamoylfosfátsyntetázy, která je v nepřítomnosti svého alosterického aktivátoru neaktivní - N-acetyl-glutamát. Koncentrace posledně jmenovaného závisí na koncentraci jeho prekurzorů (acetyl-CoA a glutamátu), stejně jako argininu, což je alosterický aktivátor N-acetylglutamátsyntázy:
Acetyl CoA + glutamátN-acetylglutamát + CoA-SH
Koncentrace enzymů ornitinového cyklu závisí na obsahu bílkovin ve stravě. Při přechodu na stravu bohatou na bílkoviny se v játrech zvyšuje syntéza enzymů ornitinového cyklu. Při návratu k vyvážené stravě se koncentrace enzymů snižuje. Za podmínek nalačno, kdy se zvyšuje rozklad tkáňových bílkovin a využití aminokyselin jako energetických substrátů, se zvyšuje produkce amoniaku a zvyšuje se koncentrace enzymů ornitinového cyklu.
24.4.4. Poruchy ornitinového cyklu. Metabolické poruchy jsou známé díky částečnému blokování každého z 5 enzymů, které katalyzují reakce syntézy močoviny v játrech, a také N-acetylglutamátsyntázy. Tyto genetické vady se zdají být dílčí. Úplné zablokování kteréhokoli kroku cyklu močoviny v játrech se zdá být neslučitelné se životem, protože neexistuje žádný jiný účinný způsob odstranění amoniaku.
Společným příznakem všech poruch syntézy močoviny je zvýšený obsah NH4 + v krvi ( hyperamonémie). Nejzávažnější klinické projevy jsou pozorovány při defektu enzymu karbamoylfosfátsyntetázy. Klinické příznaky společné všem poruchám cyklu močoviny jsou zvracení, nekoordinovanost, podrážděnost, ospalost a mentální retardace. Pokud není nemoc diagnostikována, rychle nastává smrt. U větších dětí jsou projevy onemocnění podrážděnost, zvětšení velikosti jater a nechuť k potravinám s vysokým obsahem bílkovin.
Laboratorní diagnostika chorob zahrnuje stanovení obsahu amoniaku a metabolitů ornitinového cyklu v krvi, moči a mozkomíšním moku; v těžké případy uchýlit se k jaterní biopsii.
Významné zlepšení je pozorováno při omezení bílkovin ve stravě a lze předejít mnoha mozkovým poruchám. Nízkobílkovinná dieta vede u lehkých forem těchto dědičných poruch ke snížení obsahu amoniaku v krvi a ke zlepšení klinického obrazu. Jídlo by mělo být přijímáno často, v malých porcích, aby se zabránilo prudkému zvýšení hladiny amoniaku v krvi.
24.4.5. Klinický a diagnostický význam stanovení močoviny v krvi a moči. V krvi zdravý člověk obsah močoviny je 3,33 - 8,32 mmol/l. Během dne se močí vyloučí 20-35 g močoviny.
Změny obsahu močoviny v krvi při onemocněních závisí na poměru procesů její tvorby v játrech a vylučování ledvinami. Zvýšení obsahu močoviny v krvi (hyperasotémie) je zaznamenáno při selhání ledvin, snížení selhání jater, při dietě s nízkým obsahem bílkovin.
Zvýšené vylučování močoviny močí je pozorováno při konzumaci potravin s vysokým obsahem bílkovin, při onemocněních doprovázených zvýšeným katabolismem bílkovin v tkáních, při užívání některých léků (například salicylátů). Snížení vylučování močoviny v moči je charakteristické pro onemocnění a toxické léze jater, onemocnění ledvin, doprovázené porušením jejich filtrační kapacity.
biosyntéza močoviny. Vztah mezi ornitinovým cyklem a cyklem TCA. Původ atomů dusíku močoviny. Porušení syntézy a vylučování močoviny. Hyperamonémie
Biologie a genetika
Močovina je hlavním konečným produktem metabolismu dusíku, při kterém je z těla vyloučeno až 90 % veškerého vyloučeného dusíku. Vylučování močoviny je normálně 25 g/den. Se zvýšením množství bílkovin konzumovaných s jídlem se zvyšuje vylučování močoviny.
biosyntéza močoviny. Vztah mezi ornitinovým cyklem a cyklem TCA. Původ atomů dusíku močoviny. Porušení syntézy a vylučování močoviny. Hyperamonémie.
Močovina je hlavním konečným produktem metabolismu dusíku.při kterém se z těla vyloučí až 90 % veškerého vyloučeného dusíku. Vylučování močoviny je normálně ~25 g/den. Se zvýšením množství bílkovin konzumovaných s jídlem se zvyšuje vylučování močoviny. Močovina se syntetizuje pouze v játrech. Poškození jater a porucha syntézy močoviny vedou ke zvýšení obsahu amoniaku a aminokyselin (především glutaminu a alaninu) v krvi a tkáních.
Močovina (močovina) - úplný amid kyseliny uhličité - obsahuje 2 atomy dusíku.zdroj jednoho z toho je čpavek, který se v játrech váže na oxid uhličitý za vzniku karbamoylfosfátu působením karbamoylfosfátsyntetázy I.
![]()
Dále se působením ornithinkarbamoyltransferázy karbamoylová skupina karbamoylfosfátu přenese na a-aminokyselinu ornitin a vytvoří se další a-aminokyselina, citrulin. V další reakci argininosukcinátsyntetáza váže citrulin s aspartátem a tvoří argininosukcinát (kyselinu argininosukcinovou). Tento enzym potřebuje ionty Mg2+. Při reakci se spotřebuje 1 mol ATP, ale využije se energie dvou makroergických vazeb. Aspartát je zdrojem druhého atomu dusíku močovinyDále enzym argininosukcinát lyáza (argininosukcináza) štěpí argininosukcinát na arginin a fumarát, zatímco aminoskupina aspartátu je v molekule argininu. Arginin je hydrolyzován arginázou za vzniku ornithinu a močoviny. Arginázové kofaktory jsou ionty Ca2+ nebo Mn2+. Vysoké koncentrace ornithinu a lysinu, které jsou strukturními analogy argininu, inhibují aktivitu tohoto enzymu. Výsledný ornitin interaguje s novou molekulou karbamoylfosfátu a cyklus se uzavírá. První dvě reakce procesu probíhají v mitochondriích hepatocytů. Poté je citrulin, který je produktem těchto reakcí, transportován do cytosolu, kde probíhají další přeměny.
Celková rovnice pro syntézu močoviny:
CO2 + NH3 + aspartát + 3 ATP + 2 H2O → močovina + fumarát + 2 (ADP + H3P04) + AMP + H4P2O7.
Vztah ornitinového cyklu a obecná cesta katabolismu. Fumarát, vzniklý v důsledku rozkladu argininosukcinátu, je přeměněn na malát, který je následně přenesen do mitochondrií, zahrnut do cyklu TCA a dehydrogenován za vzniku oxaloacetátu. Tato reakce je doprovázena uvolněním 3 molekul ATP, které kompenzují energetické náklady na syntézu jedné molekuly močoviny.
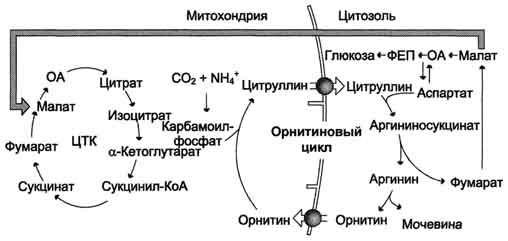
Hyperamonémie Porušení reakcí neutralizace amoniaku může způsobit zvýšení obsahu amoniaku v krvi- hyperamonémie, která má toxický účinek na tělo. Příčinou hyperamonémie může být jak genetický defekt enzymů ornitinového cyklu v játrech, tak sekundární poškození jater v důsledku cirhózy, hepatitidy a dalších onemocnění. Existuje pět známých dědičných onemocnění způsobených defektem pěti enzymů ornitinového cyklu:
Dědičné poruchy ornitinového cyklu a jejich hlavní projevy
|
Choroba |
Enzymová vada |
Typ dědičnosti |
Klinické projevy |
Metabolity |
|
|
krev |
moč |
||||
|
Hyperamonémie typu I |
Karbamoylfosfátsyntetáza I |
autozomálně recesivní |
Do 24-48 hodin po narození, kóma, smrt |
Gln Ala NH3 |
Orotat |
|
Hyperamonémie, typ II |
Ornitin karbamoyl transferáza |
X-vázaný |
Hypotenze, snížená tolerance bílkovin |
Gln Ala NH3 |
Orotat |
|
Citrulinémie |
Arginino-sukcinát-syntetáza |
autozomálně recesivní |
Hyperamonémie je u novorozenců závažná. U dospělých - po proteinové zátěži |
Citrulin NH3 |
citrulin |
|
Arginino-sukcinaturie |
Arginino-sukcinát-lyáza |
autozomálně recesivní |
Hyperamonémie, ataxie, záchvaty, vypadávání vlasů |
Argininosukcinát NH3 |
Argininosukcinát, Gln, Ala, Liz |
|
Hyperargyninémie |
argináza |
autozomálně recesivní |
Hyperargininémie |
duben NH3 |
dubna Liz Ornithine |
Porušení ornitinového cyklu je pozorováno u hepatitidy různé etiologie a některých dalších. virová onemocnění. Například byly zjištěny chřipkové viry a další akutní respirační infekce virové infekce snižují aktivitu karbamoylfosfátsyntetázy I. Při cirhóze a jiných jaterních onemocněních je také často pozorována hyperamonémie. Snížení aktivity jakéhokoli enzymu syntézy močoviny vede k akumulaci substrátu tohoto enzymu a jeho prekurzorů v krvi. Takže s defektem argininosukcinátsyntetázy se zvyšuje obsah citrulinu (citrulinémie); s defektem arginázy - koncentrace argininu, argininosukcinátu, citrulinu atd. U hyperamonémie typu I a II se v důsledku defektu ornitinkarbamoyltransferázy karbamoylfosfát hromadí v mitochondriích a vstupuje do cytosolu. To způsobuje zvýšení rychlosti syntézy pyrimidinových nukleotidů (v důsledku aktivace karbamoylfosfátsyntetázy II), což vede k akumulaci orotátu, uridinu a uracilu a jejich vylučování močí. Zvyšuje se obsah všech metabolitů, stav pacientů se zhoršuje s nárůstem množství bílkovin v potravě. Závažnost průběhu onemocnění závisí také na stupni poklesu aktivity enzymů. Všechna porušení ornitinového cyklu vedou k výraznému zvýšení koncentrace amoniaku, glutaminu a alaninu v krvi.
Hyperamonémiedoprovázené následujícími příznaky:
- nevolnost, opakované zvracení;
- závratě, křeče;
- ztráta vědomí, edém mozku (v těžkých případech);
- mentální retardace (v chronické vrozené formě
- Všechny příznaky hyperamonémie jsou projevem působení amoniaku na centrální nervový systém (viz pododdíl IV, B výše).
Pro diagnostiku různé typy hyperamonémie určují obsah amoniaku v krvi, metabolity ornitinového cyklu v krvi a moči, aktivitu enzymů v jaterních biopsiích. Hlavním diagnostickým znakem jezvýšení koncentrace amoniaku v krvi. Obsah amoniaku v krvi může dosáhnout 6000 µmol/l (normální - 60 µmol/l). Ve většině chronických případů se však hladiny amoniaku mohou zvýšit pouze po proteinové zátěži nebo během akutních komplikovaných onemocnění.
Stejně jako další díla, která by vás mohla zajímat |
|||
| 28799. | Jaké charakteristické rysy poznamenaly sociokulturní vývoj východoslovanských kmenů v 6.–9 | 19,3 kB | |
| Předkové Slovanů patřili ke staré indoevropské jednotě. Jedním z nich byli Slované. Později se ve slovanském masivu objevují západní větve Wends a východní Antes. | |||
| 28800. | Jak probíhal vznik staroruského státu? Jaké názory na tuto problematiku znáte | 21,64 kB | |
| Vznik státu východní Slované dlouhý proces natažený v čase, díky kterému se zachovaly pozůstatky kmenové demokracie. VZNIK STARÉHO RUSKÉHO STÁTU 1. K politickým faktorům formování státu u východních Slovanů patří komplikace vnitrokmenových vztahů a mezikmenové střety, které urychlily formování knížecí moci, zvýšily roli knížat a čet. jak bránit kmen před vnějšími nepřáteli, tak působit jako rozhodce v různých druzích sporů. | |||
| 28801. | Stát Kyjevská Rus a jeho civilizační rysy (sociálně-politický systém, ekonomika, legislativa, kultura) | 16,04 kB | |
| šíří v Rusku slovanské abecedy Cyrilice a hlaholice vytvořené Cyrilem a Metodějem. V Rusku se gramotnost rozšířila také v důsledku přijetí křesťanství a výskytu literatury ve slovanském jazyce. Bylo přijato křesťanství, což znamenalo zahrnutí Ruska v r křesťanství. Pro Kyjevská Rus charakteristický byl slabý právní vývoj, nerozvinutí státních principů, nedostatek jednoty, což vedlo k následnému kolapsu. | |||
| 28802. | Proč Rusko přijalo křesťanství? Jaký význam mělo přijetí křesťanství pro rozvoj země | 13,83 kB | |
| Kulturní vazby s vyspělejšími zeměmi a především s Byzancí přispěly k přijetí křesťanství. Přijetí křesťanství mělo v ruských dějinách kolosální politický a kulturní význam: 1. Vliv křesťanství na rozvoj kultury se projevil rozšířením do Ruska. Slovanské písmo rozvoj ikonografie. | |||
| 28803. | Jaké jsou důvody politické fragmentace v Rusku? Uveďte popis ruských knížectví a zemí v podmínkách decentralizace Kyjevské Rusi | 15,29 kB | |
| Příčiny: boj o moc růst měst nájezdy nomádů Kyjev ztrácí svůj význam 1Vladimir-Suzdalskaja Jurij Dolgorukov moc patřila knížeti 2galecko-volyňský princ Daniil Romanovič moc patřila bojarskému princi 3Novgorod moc veche lidové shromáždění . | |||
| 28804. | Rusko a Zlatá horda. Jaká hodnocení mongolského faktoru v dějinách Ruska existují v historické literatuře | 15,88 kB | |
| Karamzin byly následující: dohoda s Tatary, která umožnila strávit 40 let míru; velké zásluhy o svou malou vlast, moskevské knížectví: obohatil, posílil, rozšířil; LN Gumilev se domníval, že v Rusku neexistuje žádné mongolsko-tatarské jho. Batuovy invaze byly pouze vojenským nájezdem a následné události s ním neměly žádný přímý vztah. Argumentoval tím, že vladimirské velkovévodství, zastoupené Alexandrem Něvským, dosáhlo výhodného spojenectví s Zlatá horda V roce 1237 Batu napadl území Ruska. ׊títek pro vládnoucí feťáky... | |||
| 28805. | Jaké jsou důvody vzestupu Moskvy? Jaké další alternativy ke sjednocení Ruska byste mohl jmenovat? | 14,07 kB | |
| svržení mongolsko-tatarského jha Ivanem III., k němuž došlo pokojně po odmítnutí vzdát hold Hordě a následné postavení ruských a tatarských jednotek na Ugra proti sobě, když se chán neodvážil vstoupit do bitvy . první soubor zákonů nového sjednoceného ruského státu Sudebnik Ivana III. dokončení sjednocovacího procesu za syna Ivana III Basil III. | |||
| 28806. | Vznik centralizovaného Muscova v 15.–16. století. Jak se tento proces v Rusku liší od západní Evropy? | 13,91 kB | |
| Rysy politického systému moskevského království byly: a vnitřní: 1 autoritářský charakter státní moc 2 transformace Ruska od 15. století a jediný samostatný pravoslavný stát na světě; 3 upevňování politické a kulturní izolace a zaostávání za Evropou; b vnější: 1 rozsáhlé území státu 2 přeměna Ruska v mnohonárodnostní stát Závěrečná etapa centralizace ruského státu je spojena se jménem a vládou vnuka Ivana III., Ivana Hrozného, který jako první přijal v roce 1547. Tak... | |||
| 28807. | Zahraniční politika sovětského státu ve 20.-30. Proč v tomto období nebylo možné vytvořit mezinárodní bezpečnostní systém | 15,85 kB | |
| Proč v tomto období nebylo možné vytvořit mezinárodní bezpečnostní systém Zahraniční politika SSSR v roce 2030 SSSR dosáhl zrušení ekonomické blokády. 1924-1933 roky postupného uznávání SSSR Koncem 20. let došlo k prudkému zhoršení mezinárodního postavení SSSR. | |||
Způsoby vzniku amoniaku
Amoniak se tvoří ve všech tkáních, zejména v mozku, neutralizuje se v játrech a ledvinách.
Způsoby vzdělávání:
1) deaminace a/to-t;
2) deaminace purinových bází;
3) rozklad pyrimidinových bází;
4) deamidace amidů;
5) deaminace biogenních aminů;
6) rozklad hexosaminů
Deaminace- hlavní cesta rozkladu (katabolismu) a / to-t. Přibližně 70 g a/to-t je podrobeno deaminaci za den.
1) hydrolytické
2) redukční deaminace
3) intramolekulární (asp, asn a gis),
4) oxidační (tento druh je zásaditý (glu).
Proces probíhá působením enzymu - glutamátu DG, který je v aktivní formě.
Způsoby neutralizace amoniaku.
Amoniak v malých dávkách je fyziologicky dráždivý, ve velkých dávkách je to toxická látka. Proto by koncentrace amoniaku v těle měla být na nízké úrovni - 60 μM / l. Homeostáza amoniaku je udržována jeho neutralizací v tkáních.
způsoby:
1) amidace;
2) geneze amonia;
3) redukční aminace;
4) syntéza močoviny.
Amoniak, který vzniká při deamidaci v játrech, se neutralizuje a využívá se k syntéze močoviny. V ledvinách - na tvorbu amonných solí (geneze amonia). V játrech a dalších tkáních se při reakci neutralizuje amoniak redukční aminace. Převážně v játrech probíhá proces tvorby močoviny, která je hlavním způsobem detoxikace amoniaku.
Tvorba močoviny nazývaný ornitinový cyklus nebo teorie citrulinu. K syntéze močoviny dochází v MTX v játrech. Dříve v MTX v akci karbamoylfosfátsyntetáza I při spotřebě 2ATP se amoniak váže s CO2 za vzniku karbamoylfosfátu:
1.V MTH ornithinkarbamoyltransferáza převádí karbamoylovou skupinu karbamoylfosfátu na ornithin a tvoří - citrulin:
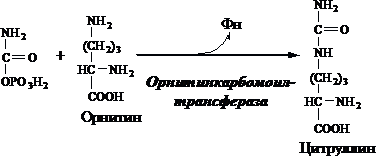
2. V cytosolu argininosukcinát syntetáza s cenou 1ATP (2 makroergické vazby) váže citrulin s aspartátem a vzniká argininosukcinát (kyselina argininosukcinová) Enzym potřebuje Mg2 + mAspartát je zdrojem 2. atomu dusíku močoviny.
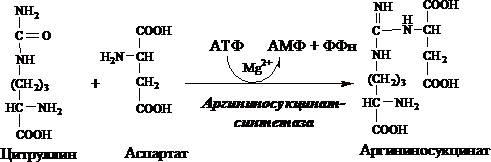
3. V cytosolu argininosukcinát lyáza (arginin sukcináza) štěpí argininosukcinát na arginin a fumarát (aminoskupina aspartátu je v argininu).
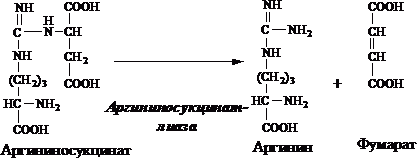
Fumarát v CTC.
4. V cytosolu argináza hydrolyzuje arginin na ornitin a močovinu. Argináza má kofaktory Ca2+ nebo Mn2+ ionty, vysoké koncentrace ornithinu a lysinu jsou inhibitory.
![]()
Výsledný ornitin interaguje s novou molekulou karbamoylfosfátu a cyklus se uzavírá. Močovina se vylučuje do krve-> ledvinami->.
Obecná rovnice pro syntézu močoviny:
CO2 + NH3 + asp + 3ATP + 2H2O → močovina + fumarát + 2ADP + AMP + 2Pn + FFn.
Pro syntézu 1 molekuly močoviny se spotřebují 4 makroergické vazby 3ATP.
Funkce cyklu:
1. Přeměňuje dusík AA na močovinu, která se vylučuje a zabraňuje hromadění toxických produktů, zejména amoniaku.
2.syntéza argininu a doplňování jeho fondu v těle.
Přestávka v cyklu:
1. Hyperamonémie typu 1 - defekt v karbomail fosfát syntetáze.
2. Hyperamonémie typu 2
3.Citrulinemie
4. Orginin sukcinatomie
5. Hyperarinémie.
Tvorba močoviny - jedna z nejdůležitějších detoxikačních funkcí jater, spočívající v přeměně toxických fragmentů molekuly proteinu na netoxickou látku. Při deaminaci a / to - t, nukleotidů a dalších dusíkatých sloučenin se játra účastní syntézy amoniaku, jehož překročení maximálních přípustných koncentrací se stává pro tělo vysoce toxickým. K detoxikaci amoniaku dochází jeho použitím pro syntézu močoviny.
Fulltextové vyhledávání:
Home > Abstrakt >Biologie
MINISTERSTVO ŠKOLSTVÍ A VĚDY
RUSKÁ FEDERACE
FEDERÁLNÍ AGENTURA PRO VZDĚLÁVÁNÍ
PACIFICKÝ STÁT EKONOMICKÝ
UNIVERZITA
Katedra strojírenských oborů a technologií šetřících zdroje
ESEJ
Podle oboru: "Řídicí systém chemicko-technologických procesů"
Téma: Proteolýza. Cyklus močoviny.
Dokončeno:
Student Gr -----PB
Kontrolovány:
Učitel
Shlicht A.G.
Vladivostok
1. Metabolismus bílkovin: obecná informace 3
2. Proteolýza 4
3. Močovinový cyklus 6
4. Močovina 8
Reference 10
1. Metabolismus bílkovin: obecné informace
Kvantitativně tvoří proteiny nejvýznamnější skupinu makromolekul. Lidské tělo o hmotnosti 70 kg obsahuje přibližně 10 kg bílkovin a většina z nich je lokalizována ve svalech. V porovnání s bílkovinami je podíl ostatních látek obsahujících dusík v těle zanedbatelný. Rovnováha dusíku v těle je proto dána metabolismem bílkovin, který je regulován několika hormony, především testosteronem a kortizolem.
V těle dospělého člověka je metabolismus dusíku obecně vyvážený, to znamená, že množství přicházejícího a odcházejícího proteinového dusíku je přibližně stejné. Pokud se uvolní pouze část nově dodaného dusíku, je bilance kladná. To je pozorováno například při růstu organismu. Záporná bilance je vzácná, hlavně v důsledku nemocí.
Proteiny získané z potravy podléhají kompletní hydrolýze v gastrointestinálním traktu na aminokyseliny, které jsou absorbovány a distribuovány v těle krevním řečištěm. 8 z 20 proteinových aminokyselin nedokáže lidské tělo syntetizovat. Tyto esenciální aminokyseliny musí pocházet z potravy.
Prostřednictvím střev a v malé míře i ledvinami tělo neustále ztrácí bílkoviny. V souvislosti s těmito nevyhnutelnými ztrátami je nutné denně přijímat s jídlem alespoň 30 g bílkovin. Tato minimální norma se v některých zemích téměř nedodržuje, zatímco v průmyslových zemích je obsah bílkovin v potravinách nejčastěji výrazně vyšší než norma. Aminokyseliny se v těle neukládají, při nadbytečném příjmu aminokyselin v játrech se oxiduje nebo využívá až 100 g aminokyselin denně. Dusík v nich obsažený se mění na močovinu a je v této formě vylučován močí a uhlíkatý skelet se využívá při syntéze sacharidů, lipidů nebo se oxiduje za vzniku ATP.
Předpokládá se, že v těle dospělého člověka se denně zničí 300-400 g bílkovin na aminokyseliny (proteolýza).Přibližně stejné množství aminokyselin je přitom obsaženo v nově vzniklých molekulách bílkovin (biosyntéza bílkovin ). Vysoký obrat bílkovin v těle je nezbytný, protože mnoho bílkovin má relativně krátkou životnost: začnou se aktualizovat několik hodin po syntéze a biochemický poločas je 2-8 dní. Ukazuje se, že klíčové enzymy intermediárního metabolismu mají ještě kratší životnost. Aktualizují se několik hodin po syntéze. Tato neustálá destrukce a resyntéza umožňuje buňkám rychle upravit hladiny a aktivity nejdůležitějších enzymů tak, aby vyhovovaly metabolickým potřebám. Naproti tomu strukturní proteiny, histony, hemoglobin nebo složky cytoskeletu jsou zvláště odolné.
Intracelulární degradace proteinů (proteolýza) probíhá částečně v liposomech. Kromě toho jsou v cytoplazmě organely, tzv. proteazomy, ve kterých jsou zničeny špatně složené nebo denaturované proteiny. Takové molekuly jsou rozpoznávány pomocí speciálních markerů.
2. Proteolýza
Proces štěpení bílkovin na volné aminokyseliny se nazývá proteolýza. K úplnému rozkladu proteinů na volné aminokyseliny je zapotřebí několik enzymů s různými specifičnostmi. Proteinázy a peptidázy jsou přítomny nejen v gastrointestinálním traktu, ale také v buňkách. Podle místa napadení molekulou substrátu se proteolytické enzymy dělí na endopeptidázy a exopeptidázy. Endopeptidázy nebo proteinázy štěpí peptidovou vazbu v peptidovém řetězci. "Rozpoznají" a vážou krátké peptidové sekvence substrátů a relativně specificky hydrolyzují vazby mezi určitými aminokyselinovými zbytky. Proteinázy jsou klasifikovány podle reakčního mechanismu. Serinové proteinázy obsahují v aktivním centru serinový zbytek, který je důležitý pro katalytické působení těchto enzymů, u cysteinových proteináz je to cysteinový zbytek atd. Exopeptidázy hydrolyzují peptidy od konce řetězce: aminopeptidázy - od N-konce, karboxypeptidázy - od C-konce. Nakonec dipeptidázy štěpí pouze dipeptidy.
Proteazomy
Protože funkční buněčné proteiny musí být chráněny před předčasnou proteolýzou, jsou některé proteolytické enzymy buňky uzavřeny v liposomech (viz str. 228). Další dobře regulovaný systém degradace proteinů je lokalizován v cytoplazmě. Skládá se z velkých proteinových komplexů (molekulová hmotnost 2~106 Da), proteazomů. Proteazomy obsahují soudkovité jádro s 28 podjednotkami a mají sedimentační koeficient 20S. Proteolytická aktivita (v diagramu znázorněna jako nůžky) je lokalizována ve vnitřním jádru 20S. Na koncích sudů jsou uzamčeny komplexními částicemi 19S, které řídí přístup k jádru.
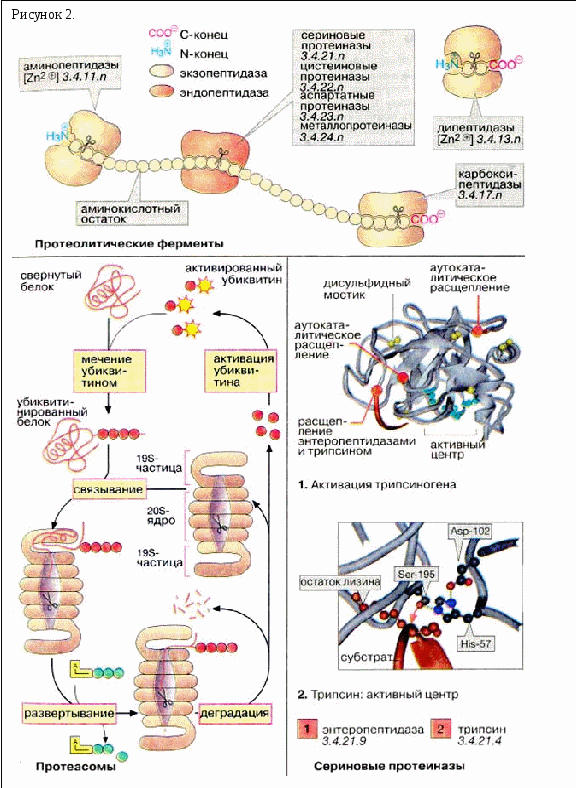
Proteiny, které mají být v proteazomu degradovány (např. ty, které obsahují transkripční chyby nebo staré molekuly), jsou značeny kovalentní vazbou na malý protein ubikvitin. Ubiquitin je aktivován díky přítomnosti thiolesterové vazby. Ub-značené („ubikvitinované“) molekuly jsou rozpoznávány částicemi 19S se spotřebou ATP a vstupují do jádra, kde jsou degradovány. Ubiquitin není zničen a po aktivaci je znovu použit.
Serinové proteinázy
Velká skupina proteináz obsahuje serin v aktivním centru. Mezi serinové proteinázy patří například trávicí enzymy trypsin, chymotrypsin a elastáza, řada faktorů srážení krve a také fibrinolytický enzym plazmin a jeho aktivátory.
Jak je znázorněno na obrázku, pankreatické proteinázy jsou vylučovány jako proenzymy (zymogeny). Aktivace takových enzymů je založena na proteolytickém štěpení. Proces aktivace je ilustrován na příkladu trypsinogenu, prekurzoru trypsinu (1). kohout začíná štěpením N-terminálního hexapeptidu enteropeptidázou ("enterokinázou"), specifickou serinovou proteinázou, která je lokalizována v membránách střevního epitelu. Produkt štěpení (β-trypsin) je enzymaticky aktivní a štěpí další molekulu trypsinogenu v místech označených na obrázku červeně (autokatalytická aktivace). Trypsinem jsou aktivovány i proenzymy chymotrypsinu, elastázy, karboxypeptidázy A aj.
Aktivní místo trypsinu je znázorněno ve schématu 2. Serinový zbytek za účasti histidinových a aspartátových zbytků nukleofilně napadá štěpitelnou vazbu (červená šipka). Štěpitelná část peptidového substrátu se nachází na C-terminální straně lysinového zbytku, jehož postranní řetězec je při katalýze fixován ve speciální „kapse“ enzymu.
3. Močovinový cyklus
Cyklus močoviny, cyklický enzymatický proces sestávající z postupných přeměn aminokyseliny ornithinu vedoucí k syntéze močoviny. Cyklus močoviny. - nejdůležitější způsob asimilace čpavku (a tím jeho neutralizace) u mnoha živočišných druhů, ale i rostlin a mikroorganismů. Nejlepší reakcí je močovinový cyklus. studovány u savců (H. Krebs a K. Henseleit, 1932 aj.), u nichž se provádějí především v játrech. Močovinový cyklus se skládá ze tří hlavních reakcí: přeměna ornithinu na citrulin, citrulinu na arginin a štěpení argininu na močovinu a ornithin.
Močovinový cyklus se vyskytuje u savců, žab, želv, žížal, ale chybí u hadů, ptáků a kostnatých ryb (funguje u žraloků). U rostlin a mikroorganismů je cyklus močoviny důležitým způsobem vázání amonných solí a jejich přeměna na organické dusíkaté sloučeniny.
K rozkladu aminokyselin dochází především v játrech. Tím se přímo nebo nepřímo uvolňuje amoniak. Při rozkladu purinů a pyrimidinů vzniká značné množství amoniaku.
Amoniak (na obrázku vlevo nahoře), středně silný základ, je buněčný jed. Při vysokých koncentracích škodí hlavně nervové buňky. Proto musí být čpavek rychle inaktivován a vyloučen z těla. V lidském těle je to dáno především tvorbou močoviny (ve schématu uprostřed vlevo), část NH 3 je vylučována přímo ledvinami.
V odlišné typy U obratlovců dochází k inaktivaci a vylučování amoniaku různými způsoby. Živočichové žijící ve vodě vypouštějí čpavek přímo do vody; např. u ryb je vylučován žábrami (amoniotelické organismy). Suchozemští obratlovci včetně člověka vylučují pouze malé množství amoniaku a většina se přeměňuje na močovinu (ureotelové organismy). Ptáci a plazi se naopak tvoří kyselina močová, který se z důvodu úspory vody uvolňuje převážně v pevné formě (urikotelové organismy).
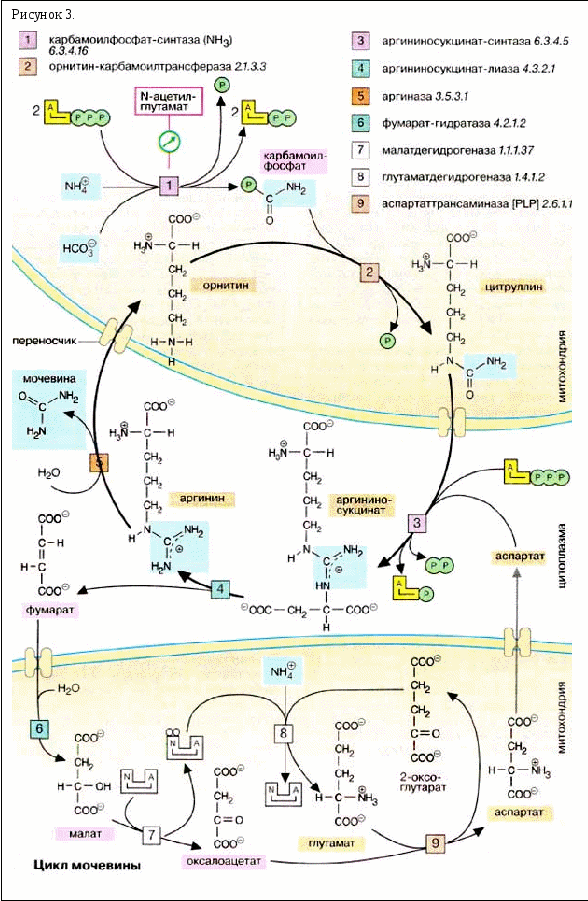
Močovina se tvoří jako výsledek cyklického sledu reakcí probíhajících v játrech. Oba atomy dusíku jsou převzaty z volného amoniaku a díky deaminaci aspartátu je karbonylová skupina převzata z hydrogenuhličitanu. V první fázi reakce z hydrogenuhličitanu (HCO 3 -) a amoniaku se spotřebou 2 molekul ATP vzniká karbamoylfosfát. Jako anhydrid má tato sloučenina vysokou reaktivitu. V dalším kroku reakce se karbamoylový zbytek přenese na ornithin za vzniku citrulinu. Druhá aminoskupina molekuly močoviny je dodávána reakcí aspartátu (v diagramu vpravo dole) s citrulinem. Tato reakce opět vyžaduje energii ve formě ATP, která se následně štěpí na AMP a difosfát. Pro zajištění nevratnosti reakce je difosfát zcela hydrolyzován (není znázorněno). Odštěpením fumarátu z argininosukcinátu vzniká arginin, ze kterého hydrolýzou vzniká izomočovina, která se přesmykem okamžitě mění na močovinu. Zbývající ornitin je znovu zaveden do cyklu močoviny.
Fumarát vzniklý v močovinovém cyklu může v důsledku dvou fází citrátového cyklu přejít přes malát na oxalacetát, který je díky transaminaci dále přeměněn na aspartát. Ten je rovněž znovu zapojen do cyklu močoviny.
Biosyntéza močoviny vyžaduje hodně energie. Potřebnou energii dodává štěpení čtyř vysokoenergetických vazeb: dvou při syntéze karbamoylfosfátu a dvou (!) při tvorbě argininosukcinátu (ATP → AMP + PPi, PPi → 2Pi).
Cyklus močoviny probíhá výhradně v játrech. Dělí se na dva kompartmenty, mitochondrie a cytoplazmu. Průchod přes membránu intermediárních sloučenin citrulinu a ornithinu je možný pouze za pomoci nosičů. Obě aminokyseliny jsou nebílkovinného původu.
Rychlost syntézy močoviny je určena první reakcí cyklu. Karbamoylfosfátsyntáza je aktivní pouze v přítomnosti N-acetylglutamátu. Metabolický stav (hladiny argininu, dodávka energie) je vysoce závislý na koncentraci tohoto alosterického efektoru.
4. Močovina
Močovina, močovina, H3NCONH3, úplný amid kyseliny uhličité, amid kyseliny karbamové; bezbarvé krystaly (t.t. 132,7°C), snadno rozpustné ve vodě, alkoholu, kapalném amoniaku, oxidu siřičitém. Objeven francouzským chemikem I. Ruellem (1773) v moči, identifikovaný anglickým chemikem W. Proutem (1818), poprvé syntetizován F. Wöhlerem (1828) zahříváním kyanátu amonného NH5NCO. Právě tento objev zasadil první ránu idealistické vitalistické doktríně o takzvané životní síle. Močovina je vysoce reaktivní sloučenina; tvoří s mnoha látkami komplexní sloučeniny, např. s peroxidem vodíku CO (NH 2) 2 ·H 2 O 2, s normálními nasycenými uhlovodíky; posledně jmenovaná reakce se používá v průmyslu pro odparafínování olejů (viz také Inkluzní sloučeniny). Při zahřátí na 150-160 °C se močovina rozkládá za vzniku biuretu H 2 NCONHCONH 2, NH 3, CO 2 a dalších produktů; při zahřívání vodných roztoků pomalu hydrolyzuje na CO 2 a NH 3 (za přítomnosti kyselin a zásad rychle), s kyselinami (HNO 3, HCl aj.) dává soli, např. CO (NH 2) 2 HNO 3 . během alkylace. alkylmočoviny RNHCONH 2 vznikají při acylaci - ureidy RCONHCONH 2, při interakci s alkoholy - urethany H 2 NCOOR. M. snadno kondenzuje s formaldehydem. Atom vodíku ve skupině NH 2 může být také nahrazen atomy halogenu (F, Cl 2).
Močovina. - konečný produkt metabolismu bílkovin u většiny obratlovců a lidí. Nachází se v krvi, svalech, slinách, lymfě, mléce a dalších tekutinách a tkáních (normální obsah v lidské krvi je 18-38 mg/100 ml). Biosyntéza močoviny z finální produkty k štěpení bílkovin - NH4 a CO 2 - dochází v játrech v důsledku řady biochemických reakcí - močovinový cyklus, neboli ornitinový cyklus (M. a ornitin vznikají při enzymatickém štěpení aminokyseliny argininu). U zvířat, která vážou NH 3 na kyselinu močovou, dochází ke ztrátě ornitinového cyklu.
Močovina. podílí se na regulaci vodního režimu živočichů: udržuje tkáňovou hypertonicitu (žraločí ryby) a zajišťuje jejich hydrataci (suchozemští živočichové). Močovina. vylučují se ledvinami a potními žlázami (člověk vyloučí asi 25-30 g denně). Obsah močoviny v moči závisí na množství a složení bílkovin v potravě, na úrovni odbourávání bílkovin (zvyšuje se při fyzické práci, horečka, cukrovka). Při poruše funkce ledvin a onemocněních spojených se zvýšeným odbouráváním tkáňových bílkovin obsah močoviny. zvýšení v krvi.
V průmyslu močovina. získané z amoniaku a oxidu uhličitého (160-200 °C, 100-400 at):
2NH4 + CO2 ® H3NCONH3 + H3O.
Nachází široké uplatnění. močovina - surovina získat karbamidové pryskyřice, stejně jako hnojiva, kyanáty, hydrazin, kyselinu kyanurovou a její estery, některá barviva, hypnotika (například veronal, luminal, bromural); v lékařské praxi močovina. pure se používá jako dehydratační činidlo k prevenci a snížení mozkového edému atd.
proteolýza Testovací práce >> Biologie
Nervy. Tajemství cyklus folikuly - V sekreci cyklus rozlišují se dva folikuly ... pomocí lysozomálního aparátu jsou proteolýza a z molekul fagocytovaných ... (0,6 %), chlorid sodný (0,5 %), nečistoty močovina cholena a těkavé mastné kyseliny...







